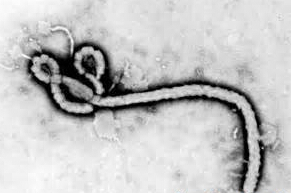
美国医药巨头强生(JNJ)近日宣布,美国食品和药物管理局(FDA)已授予该公司的Idylla埃博拉病毒分类检测试剂盒(IdyllaEBOVTest)紧急使用授权(EmergencyUseAuthorization,EUA)。医药产品紧急使用授权(EUA)指由FDA在实际的或潜在的紧急状态下对未获批准的医药产品的使用及已获批准产品的未获批准用途的授权。
IdyllaEBOVTest是一款诊断试剂盒,用于伴有埃博拉病毒感染迹象和症状的患者,检测埃博拉扎伊尔病毒(EbolaZairevirus)的存在。该试剂盒由强生旗下杨森诊断和BiocartisNV公司联合开发。
自40年前发现以来,2014年在西非爆发的埃博拉疫情是迄今为止最大的埃博拉疫情,此次疫情所导致的死亡病例超过1.1万例,并且影响西非多个国家。此次疫情,再次突显了对提高传染病监测和管理的明确需求。当前,迫切需要开展更多的针对埃博拉病毒疫情的准备工作,因为有专家预计,在未来,零星的埃博拉病毒疫情将继续发生。
Idylla埃博拉病毒分类检测试剂盒(IdyllaEBOVTest)是一种实时逆转录聚合酶链反应(rRT-PCR)检测方法,联合流行病学风险因素,对来自伴有埃博拉病毒感染迹象和症状患者的EDTA抗凝静脉全血中埃博拉扎伊尔病毒(在2014年西非疫情爆发时检测到)的RNA进行定量检测。这是一种高度标准化、自动化的试剂盒,不需要冷链储存,能够在100分钟内得出检测结果,而且只需简单培训即可对数据进行准确的解读。
强生表示,非常高兴FDA授予IdyllaEBOVTest紧急使用授权(EUA),该公司将动员全部的资源和专业知识,帮助预防下一次埃博拉病毒的爆发。
埃博拉病毒(Ebola)是导致埃博拉出血热(EHF)的元凶,该病是一种急性病毒性出血性传染病,症状包括:发烧、头痛、关节和肌肉疼痛、乏力、腹泻、呕吐、胃痛、食欲不振及异常出血。这些症状可在病毒感染后2-21天内出现,但最常见于8-10天。埃博拉病毒不是一种经水传播(water-borne)或食物传播的疾病,也不通过空气传播,该病通过直接接触受感染者体液或已被病毒污染的器具(如针头)传播。
原标题:FDA授予强生埃博拉病毒检测试剂盒(Idylla EBOV Test)紧急使用授权(EUA)
推荐阅读:3D打印定制化CPAP面罩治疗阻塞性睡眠呼吸暂停,获种子投资

本文转载自其他网站,不代表健康台观点和立场。如有内容和图片的著作权异议,请及时联系我们(邮箱:jkcentv@163.com)
责任编辑:邹林梅


相关文章



