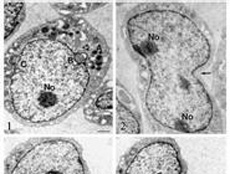
来自日本北海道大学(Hokkaido University)的一个科学家团队发现了高侵袭性乳腺癌细胞内线粒体运动并影响侵袭性的相关分子途径。研究表明,阻断这一途径,可以降低癌症的侵袭性和对放射治疗的抵抗力。
研究结果以“Arf6-driven cell invasion is intrinsically linked to TRAK1-mediated mitochondrial anterograde trafficking to avoid oxidative catastrophe”为题发表在《Nature Communications》杂志上。
众所周知,当不同类型的细胞移动时,线粒体会在细胞质中重新定位。例如,它们聚集在白细胞向外来入侵者移动的尾端,以及癌细胞入侵的前沿。细胞表面一种叫做整合素的粘附蛋白,也被认为能促进癌症侵袭性。然而,这些运动背后的机制尚不完全清楚。
当线粒体的分子途径被阻断后,线粒体在细胞中心聚集,在那里它们开始产生过量活性氧(ROS)。ROS可以增强癌症侵袭性,但过量会导致癌细胞死亡。
研究人员希望研究癌细胞内的线粒体运动,以及这些运动、整合素和ROS之间的关系,所有这些运动都与癌症侵袭有关。
在最新研究中,研究小组用荧光化合物标记了浸润性乳腺癌细胞内的各种分子,以跟踪线粒体运动和ROS的产生。然后他们阻断了已知与入侵有关的关键分子。
他们发现,促进细胞内整合素循环的分子途径——Arf6-AMP1-PRKD2也促进线粒体的定位。整合素的积累导致细胞膜上粘附复合物的形成,最终诱导线粒体向细胞边缘转移。阻断这一途径会导致线粒体在细胞中心附近聚集,从而降低癌细胞侵袭性。在实验过程中,研究团队还直接修改了线粒体的分布方式,发现线粒体聚集本身导致了过量ROS的产生,从而导致癌细胞死亡。一些治疗方法如电离辐射会增加癌细胞内ROS的产生,有助于抗癌。但是一些癌细胞会对ROS产生耐受性,从而降低抗癌效果。
这些发现表明,有利于线粒体扩散的途径使癌细胞对试图通过增加ROS的产生来杀死细胞的治疗更具抵抗力。
据研究人员称,细胞运动和线粒体动力学之间存在新的分子联系,这对于高侵袭性癌症的侵袭活性和对活性氧的耐受性都显得至关重要。研究发现也可能会带来提高ROS介导的癌症治疗效果的新策略。

本文转载自其他网站,不代表健康台观点和立场。如有内容和图片的著作权异议,请及时联系我们(邮箱:jkcentv@163.com)
责任编辑:邹林梅


相关文章